Folytatás a III. rész után.
A teljes megoldást az aszimptotikus függvény és az x változó polinomjának szorzata adja meg. Az egyenletben szereplő ε = m.e2.r0/ℏ2 mennyiség olyan értékét keressük, amikor a polinom szorzata az aszimptotikus függvénnyel reguláris (tehát véges értékű) megoldást ad . Az itt nem közölt számítások szerint a megoldás ε = n egészszám lesz, amely legalább eggyel nagyobb az l impulzusmomentum kvantumszámnál, azaz n ≧ l+1. Az n kvantumszám határozza meg a karakterisztikus sugarat r0 = a0.n, ahol a0 = ℏ2/(m.e2) az un. Bohr sugár, amit az energia kifejezésébe helyettesítve azonos eredményt kapunk, mint amit Bohr klasszikus úton levezetett.
A Schrödinger-egyenlet tehát azonos eredményre vezet, mint Bohr körpályás modellje, amikor az energiáról van szó, de alapvetően eltér az impulzusmomentum és az energia kapcsolata: ugyanakkora En energiához különböző nagyságú pálya-impulzusmomentumok tartozhatnak, melyek értéke mindig kisebb, mint n.ℏ és a nulla is megengedett. Ez egyébként a kvantummechanikai megfelelője annak a klasszikus fizikai törvénynek, hogy centrális térben a bolygók különböző elliptikus pályákon mozoghatnak azonos energia esetén is. A Bohr modellben tiltott nulla impulzusmomentumú pályák fellépése azt jelenti, hogy az elektron áthaladhat az atommagon. Ez szintén megengedett bolygómozgás esetén, de ekkor a bolygó megsemmisül, szemben az elektronnal, amelyik nem lép olyan kölcsönhatásba az atommaggal, amely megakadályozná az elektron centrumon való áthaladását. Az elektron kinetikus energiájához ezért kétféle mozgás ad járulékot, az egyik a sugár koordináta (oszcilláció), a másik a szög koordináták terében (keringés) halad. Az n = 1 fő kvantumszámmal jellemzett pályán l = 0, tehát alapállapotban nincs is keringő mozgás, ekkor csak oszcillációs jellegű mozgásról beszélhetünk, azaz a pálya áthalad az atommagon. A kvantummechanika nyelvén ez azt jelenti, hogy az l = 0 állapotok (un. „s” pályák) sűrűsége nem nulla a centrumban. Az ehhez tartozó energia E1 = – ½m.e4/ℏ2 = – ½e2/a_0 párhuzamba hozható az oszcillátorok zérusponti energiájával, de ennek értéke negatív szemben az oszcillátorok pozitív energiaskálájával. Ennek oka, hogy a molekulavibrációknál nem vettük figyelembe az atomok közötti negatív kötési energiát, és az energia nulla pontját a rezgésmentes állapothoz rögzítettük, ahol a potenciális energiának minimuma van.
A klasszikus bolygómozgással szemben, ahol minden pillanatban meg tudjuk mondani a tartózkodási helyet, a sebességet és a gyorsulást, a kvantummechanika csak a tartózkodási valószínűséget valamint a sebesség és a gyorsulás várhatóértékét adja meg az állapotfüggvény segítségével. Az n és l kvantumszámokhoz tartozó függvényeket a Pln(x) Laguerre polinomok építik fel. A hullámfüggvény alakja:
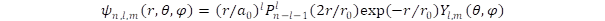
A Laguerre polinom foka n–l–1, amelynek maximális értéke n–1. Az origóban, azaz a mag helyén élesen elkülönül az l = 0 (ezeket hívjuk s pályáknak) és az l > 0 (p, d, f …) pályák térszerkezete. Az előbbi a magban nullától különböző sűrűséggel rendelkezik, mert a Laguerre polinom értéke nem nulla az origóban, míg az utóbbi esetben az rl tényező miatt az állapotfüggvény itt zérus lesz. Ez megfelel az impulzusmomentum definíciójának, hiszen ha véges valószínűséggel tartózkodna az elektron a magban, akkor csak nulla lehetne az impulzusmomentum, míg ha van impulzusmomentum, akkor nem tartózkodhat az objektum a forgás középpontjában.
Az n és l kvantumszámú „nl” pályák térbeli eloszlását a Laguerre polinomok határozzák meg. Az oszcilláció egy-dimenziós mozgásával ellentétben az elektron háromdimenziós térben mozog az atommag környezetében, ezért annak valószínűségét, hogy az s elektron a magtól valamilyen r távolságban tartózkodik, úgy számítjuk ki, hogy szorozzuk a valószínűségsűrűséget a gömb 4r2.π felszínével. Az ennek megfelelő valószínűség eloszlást a mutatja az ábra:

Az 1s (piros), 2s (fekete) és 3s (kék) pályák valószínűség eloszlása Bohr sugár egységben
Az 1s pálya (n = 1, l = 0) eloszlási valószínűségének egy maximuma van hasonlóan a harmonikus oszcilláció n = 0 alapállapotához, a maximumok száma tekintetében azonosság van a 2s pálya (n = 2, l = 0) és az oszcilláció n = 2 módusa, illetve a 3s pálya (n = 3, l = 0) és az oszcilláció n = 4 módusa között. Szintén hasonlóság van a harmonikus oszcillációval abban a tekintetben, hogy ott is a külső módus amplitúdója a legnagyobb. Az ábrán látható, hogy a külső módusok távolsága a fő kvantumszám négyzetével arányosan növekszik és egyre diffúzabbá válik. Ezek a tulajdonságok avval függnek össze, hogy a vonzóerő kis távolságokban veszi fel a nagyobb értéket és csökken az atommagtól távolodva.
Az eloszlási maximumok száma a fő kvantumszámmal egyezik meg, a csomópontok száma (nulla helyeké) n – 1 lesz, a megtalálási valószínűség nulla a centrumban, és a több módusú eloszlásokban az elektron a külső tartományban tartózkodik a legnagyobb valószínűséggel. Nagy n kvantumszámoknál a belső módusok súlya erősen lecsökken, hasonlóan az oszcillációk esetével. A nullától különböző l értékkel rendelkező pályák közül az l = n–1 pálya radiális függvénye könnyen megadható, mert ekkor a Laguerre polinom nullafokú. Az állapotfüggvény:

A radiális függvény négyzete adja meg az elektron valószínűségsűrűségét egy adott távolságban, amit az n = 2, l = 1 (2p pálya), n = 3, l = 2 (3d pálya) és n = 4, l = 3 (4f pálya) esetén mutat meg a következő ábra

Az 2p (piros), 3d (fekete) és 4f (kék) pályák valószínűségsűrűsége Bohr sugár egységben
Folytatás az V. részben: : "Miért diszkrétek az energianívók kötött állapotban_V"
További bejegyzések összefoglalója: "Paradigmaváltás a fizikában"


